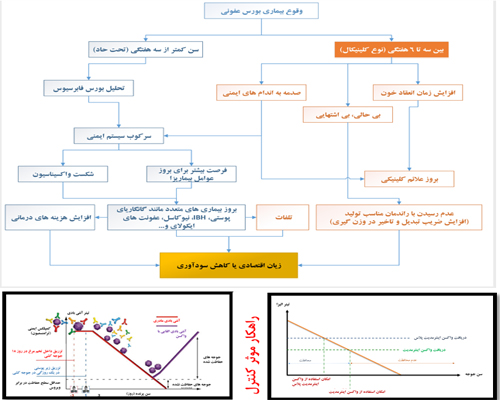
اهمیت کنجاله سویا در تغذیه طیور و بررسی شاخص های کیفی آزمایشگاهی
Стати Верстальником
2020/10/27Football Betting Sites Not On Gamstop
2020/11/04اهمیت کنجاله سویا در تغذیه طیور و بررسی شاخص های کیفی آزمایشگاهی

تیم علمی _ تحقیقاتی شرکت لعل حیات وسام
دکتر فخرالدین عابد، دکتر تیمور لطیفی، مهندس ضیا الدین عابد، خانم دکتر محمدپور* و خانم جهاندار
* نویسنده مسئول: mohammadpour_68@yahoo.com
چکیده
لوبیای سویا یک منبع روغن با کیفیت بالا در تغذیه انسان و یک منبع پروتئین گیاهی با کیفیت در تغذیه حیوانات به خصوص در صنعت طیور می باشد. از دلایل منحصر بفرد بودن این ماده خوراکی در صنعت طیور می توان به موارد زیر اشاره کرد:
- محتوای پروتئین نسبتاً بالا
- پروفایل اسیدآمینه مناسب به جز کمبود آن در رابطه با اسیدآمینه متیونین
- میزان تریپتوفان بالا
- قابلیت هضم بالای لیزین به عنوان یک ماده غذایی با قابلیت برطرف کنندگی کمبود های دانه غلات در میزان لیزین
- محتوای فیبر خام پایین در مقایسه با دیگر منابع پروتئین گیاهی
- مقرون به صرفه بودن نسبت به سایر مواد پروتئینی
- قابل کنترل بودن فاکتورهای ضدتغدیه ای (ANFs) [1] در صورتی که به درستی فرآوری شده باشد
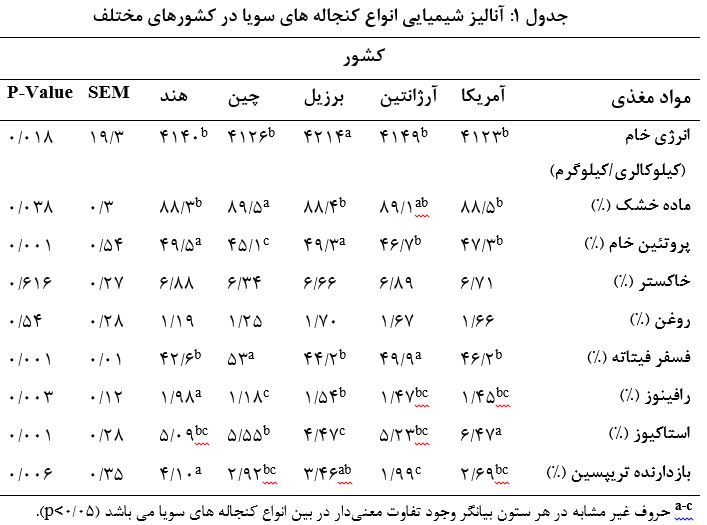
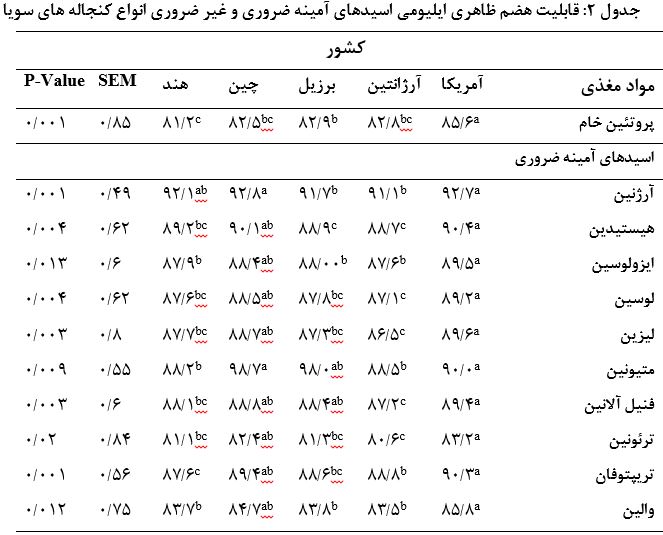
کنجاله سویا یک محصول جانبی از استخراج روغن از دانه سویا بوده بنابراین نوع فرآوری محصولات مختلفی به وجود می آورد. ارزش تغذیه ای کنجاله سویا تابع تفاوت های ژنتیکی به دلیل نوع واریته دانه سویا، شرایط آب و هوایی مختلف، نوع خاک و شرایط فرآوری است. بنابراین انواع مختلف کنجاله های سویا با توجه به کشور تولید کننده تقسیم بندی می شوند. بر اساس یک مطالعه آنالیز شیمیایی انواع کنجاله ها مورد مطالعه قرار گرفت و نتایج حاصل از میزان مواد مغذی و همچنین قابیلت هضم پروتئین و اسیدهای آمینه هز کدام از کنجاله ها در جدول ۱ و ۲ ارائه شده است (۱). بر اساس آمار جهانی، ایالت متحده آمریکا حدود ۳۴ درصد، برزیل حدود ۲۹ درصد، آرژانتین حدود ۱۹ درصد و چین حدود ۶ درصد از کل تولیدات سویای جهان را به خود اختصاص می دهند.
در یک تقسیم بندی دیگر بر اساس میزان پروتئین دو نوع سویا با پروتئین بالا (۴۹-۴۵ درصد) و فیبر پایین که بدون پوست می باشد (SBM-HP) [2] و سویا با پروتئین متوسط (۴۴-۴۳ درصد) و فیبر نسبتاً بالاتر (SBM-CV) [3] در بازار موجود است. بر خلاف نقش حیاتی سویا در صنعت طیور، به دلیل وجود فاکتورهای ضدتغذیه ای و تأثیر منفی آنها بر کیفیت سویا و متعاقباً بر عملکرد طیور، قابلیت استفاده به صورت خام ندارد. اما زمانی که تحت شرایط فرآوری مناسب قرار گیرد، برخی از آنها به یک سطح بی خطر تبدیل خواهند شد (۲). بنابراین در ادامه با بررسی این موضوع مهم سعی بر این داریم تا مطالبی در این خصوص در اختیار افراد دخیل در صنعت طیور قرار دهیم.
فاکتورهای ضدتغذیه ای در کنجاله سویا
فاکتورهای ضدتغذیه ای در کنجاله سویا را میتوان به دو دسته تقسیم کرد (۳):
۱: فاکتور های ضدتغذیهای حساس به حرارت: شامل بازدارنده تریپسین، لکتین و گوآتروژن
۲: فاکتور های ضدتغذیه ای مقاوم به حرارت: شامل الیگوساکاریدها، اسیدفایتیک (فیتات)، و آنتی ژن ها، تانن، فیتواستروژن ها و ساپونین ها. این دسته از فاکتورهای ضد تغذیه ای (به جز الیگوساکارید ها، فیتات و آنتی ژن ها) در دانه سویا بسیار پایین بوده و منجر به مشکلات جدی در تغذیه طیور نمی شوند.
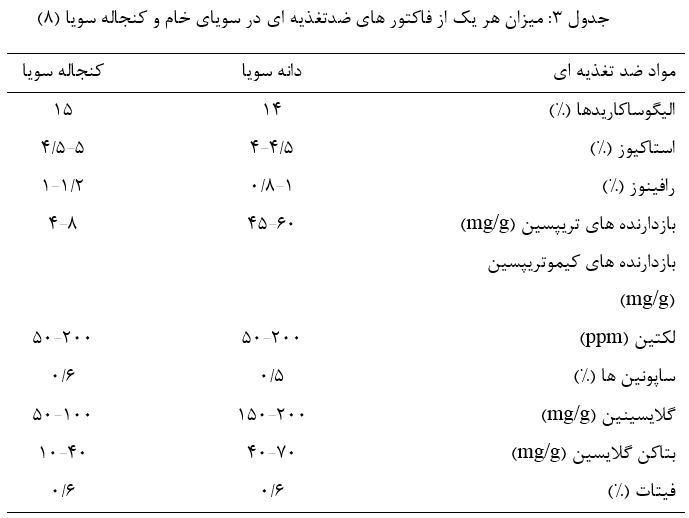
میزان هر یک از فاکتورهای ضدتغذیهای در دانه سویای خام و کنجاله سویا در جدول ۳ ارائه شده است.
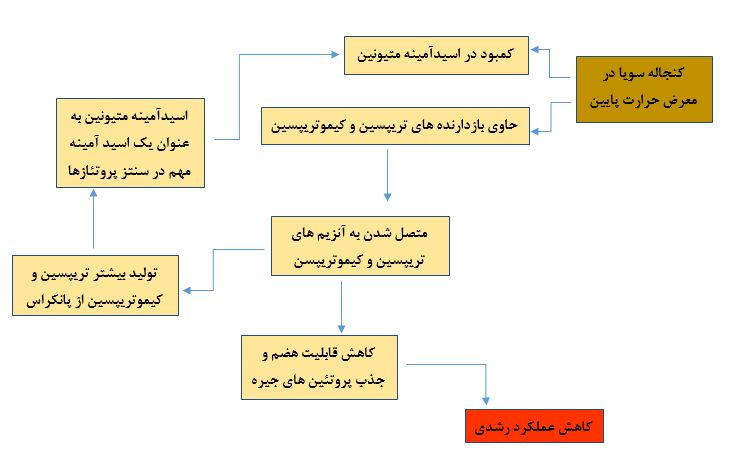
بازدارنده تریپسین
از جمله مهمترین فاکتور های ضدتغذیه ای موجود در دانه خام سویا بازدارندگان تریپسین و کیموتریپسین می باشند. این بازدارنده ها به وسیله تشکیل کمپلکس غیر قابل هضم با آنزیم های پروتئاز تریپسین و کیموتریپسین مانع از هضم و جذب پروتئین های جیره شده که متعاقب آن سبب کاهش ابقای نیتروژن و افزایش دفع نیتروژن، کاهش عملکرد پروتئاز های پانکراس، بزرگ شدن پانکراس (افزایش در سایز و تعداد سلول های پانکراس) و کاهش عملکرد رشدی در طیور خواهد شد. فعالیت این بازدارنده ها با استفاده از حرارت تا بیش از ۹۰ درصد کاهش می یابد. حساسیت به این بازدارنده ها در بین حیوانات متفاوت بوده و جوجه های گوشتی بیشترین حساسیت را به این بازدارنده ها دارند (۴).
لکتین
لکتین ها (هماگلوتینین ها- باند کننده های گلبول های قرمز خون) پروتئین هایی هستند که با کربوهیدرات ها باند می شوند. بر اساس تحقیقات انجام شده بازدارندگان تریپسین مسئول ۴۰ درصد از کاهش رشد مشاهده شده در جوجه های تغذیه شده با دانه خام سویا بوده در حالیکه حدود ۱۵ درصد کاهش رشد مشاهده شده در جوجه های گوشتی را مربوط به لکتین ها گزارش کرده اند. لکتین موجود در دانه خام سویا مانع اثر آمیلاز پانکراس در اپیتلیوم روده شده و دفع آن را از طریق مدفوع تسریع می کند که این مسئله می تواند سبب کاهش قابلیت هضم نشاسته جیره شود. گزارش شده است که لکتین موجود در کنجاله سویا منجر به آسیب هایی در ژژنوم شده و همچنین با اتصال به دیواره روده مانع از جذب مواد مغذی نیز می شوند (۴).
پروتئین های آلرژن (آنتی ژن ها)
اثرات آلرژیکی دانه سویا مربوط به بخش گلوبولین پروتئین های سویا می باشد. گلوبولین ها حدود ۸۵ درصد از کل پروتئین های دانه سویا را تشکیل می دهند. مهمترین آلرژن های دانه سویا شامل گلایسین و بتا کن-گلایسینین و گاما کن- گلایسین است که منجر به تحریک سیستم ایمنی و تولید آنتی بادی هایی در سرم حیواناتی مانند گوساله، خوک و انسان می شود. همچنین منجر به جلوگیری از تکثیر باکتری های مفید در دستگاه گوارش خواهد شد. روش های تشخیص این ترکیبات استفاده از الکتروفورز و کروماتوگرافی مایع با کارایی بالا (HPLC) می باشد (۵).
الیگوساکاریدهای غیر قابل هضم
اگرچه کنجاله سویا دارای مزایای بسیاری است اما انرژی متابولیسم کمتری در مقایسه با پیش بینی انرژی ناخالص یا انرژی کل (Gross energy) برای طیور است که تا حدی به دلیل قابلیت هضم پایین الیگوساکاریدها در آن است، که به طور بالقوه می تواند منجر به اتلاف انرژی زیاد در رژیم غذایی شود. گالاکتوالیگوساکاریدها تقریباً ۱۱ درصد از ماده خشک آن را تشکیل می دهند. از جمله مهمترین الیگوساکاریدهای موجود در کنجاله سویا رافینوز و استاکیوز و ورباسکیوز می باشند. رافینوز یک تری ساکاریدی است که واحدهای گالاکتوز با پیوند آلفا ۱-۶ به واحدهای گلوکز ساکارز متصل هستند.
استاکیوز نیز یک تترا ساکارید است که حاوی یک واحد گالاکتوز باند شده (آلفا ۱-۶) با یک واحد رافینوز می باشد. به دلیل عدم وجود آنزیم های تجزیه کننده این کربوهیدرات ها در روده کوچک طیور قابل تجزیه نبوده و قادر به عبور از دیواره روده نیستند. بنابراین این الیگوساکاریدها از قسمت بالایی دستگاه گوارش عبور کرده و به قسمت های تحتانی دستگاه گوارش توسط باکتری های بی هوازی مورد تخمیر قرار می گیرند محصولات تخمیر شامل کربن دی اکسید، متان و هیدروژن می شوند که منجر به اختلالات گوارشی در حیوانات می شود. علاوه بر این، اگر غلظت این الیگوساکاریدها در دستگاه گوارش زیاد باشد، ممکن است باعث احتباس مایعات و افزایش چسبندگی محتویات هضمی روده و کاهش هضم فیبر و در نتیجه پایین آمدن مقدار انرژی متابولیسمی شوند (۶) (۷).
فیتات
کیلات های اسید فایتیک کلیسم، منیزیوم، پتاسیم، آهن، روی، منجر به غیرقابل دسترس کردن این مواد برای حیوانات تک معده ای می شود. همچنین فیتات منجر به کاهش فعالیت آنزیم ها (پپسین، تریپسین و آمیلاز) شده و همچنین قابلیت دسترسی به پروتئین، اسیدهای آمینه و نشاسته را کاهش می دهد. فیتات ها منجر به کاهش مصرف خوراک و بنابراین کاهش رشد جوجه های گوشتی می شود. تخمین زده شده است که حدود دو سوم از فسفر موجود در سویا با فیتات باند شده است (۸). علاقه مندان به مطالعه بیشتر در رابطه با انواع فیتازها و نحوه عملکرد هر کدام می توانند به لینک زیر تحت عنوان عملکرد فیتازهای مختلف از لوله آزمایش تا لوله گوارش در سایت شرکت لعل حیات وسام مراجعه فرمایند.
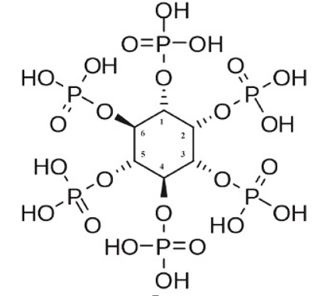
کنترل کیفی مواد خام یک رکن مهم در تمام صنایع به خصوص صنعت خوراک حیوانات می باشد. بنابراین توجه به برنامه های کنترل کیفی مواد خام منجر به افزایش کیفیت محصول نهایی خوراک حیوانات و در نهایت افزایش کیفیت غذای انسان خواهد شد. دانه خام سویا حاوی تعداد زیادی فاکتورهای ضد تغذیه ای است که منجر به کاهش ارزش تغذیه ای و عملکرد رشد و سلامت حیوان به خصوص حیوانات تک معده ای از جمله جوجه های گوشتی می شود.
تأثیر تکنولوژی فرآوری خوراک بر ارزش تغذیه ای سویا و فرآورده های آن
ارزش تغذیه ای سویا را می توان با استفاده از روش های مانند پختن، اکسترود کردن، تخمیر، خیساندن و تیمار کردن با اوره که منجر به غیرفعال شدن برخی از این فاکتور ها می شود افزایش داد. حجم بالایی از تولید کنجاله سویا به وسیله استخراج روغن توسط یک حلال و سپس اعمال حرارت به منظور حذف کامل حلال و تجزیه فاکتورهای ضد تغذیه انجام می شود. کارایی این روش به شدت و مدت دمای اعمال شده بستگی دارد. بنابراین میزان حرارت و طول مدت حرارت اعمال شده در این مرحله بسیار بحرانی و مهم می باشد. به گونه ای که در صورت فرآوری حرارتی درست قابلیت دسترسی به لیزین، متیونین و سیستئین در کنجاله سویا افزایش می یابد، در مقابل، اعمال دمای بالا منجر به کاهش قابلیت دسترس پروتئین و برخی از اسیدهای آمینه به خصوص لیزین می شود (۹).
لیزین به عنوان حساس ترین اسیدآمینه به حرارت می باشد که گروه ۳- آمین آن در واکنش میلارد درگیر می شود (شکل ۱). لیزین همچنین با شاخه جانبی سایر اسیدهای آمینه از جمله سیستئین برای تشکیل لیزینوآلانین واکنش می دهد. همچنین حرارت دهی ملایم (حدود ۹۰ درجه سانتی گراد) به وسیله دناتوره کردن پروتئین منجر به ایجاد مکان های جدید برای هیدورلیز آنزیمی می شود. بنابراین حرارت کافی در کیفیت کنجاله سویا بسیار حائز اهمیت است و قابلیت هضم پروتئین در بین کنجاله های سویا به دلیل شرایط فرآوری متفاوت می تواند بسیار متغیر باشد. از طرفی اعمال حرارت بالا منجر تبدیل فرم L اسیدهای آمینه به فرم –D انانتیومر (Racemization) در پروتئین های موجود در کنجاله سویا شده که قابلیت دسترسی ضعیف تری دارند (۱۰). همچنین میزان حلالیت پروتئین کنجاله سویا نیز در زمانی که کنجاله سویا در معرض دمای بالا قرار گرفته باشد کاهش می یابد.

واکنش میلارد یک سری از واکنش های پیچیده ای است که در اثر فرآوری حرارتی بالا در کنجاله سویا اتفاق می افتد. که شامل مراحل ابتدایی، پیشرفته و نهایی می باشد. ترکیبات هتروسیلیک (پیرازین، پیرولز، پیریدین ها و تیازول ها) در آخرین مرحله تشکیل می شود که به صورت رنگ تیره به دلیل رنگدانه های ملانودین قهوه ای در خوراک می باشد.
مهمترین چالش در رابطه با کیفیت کنجاله سویا به کار بردن زمان و شدت دمای بهینه برای دستیابی به یک کنجاله سویا با ارزش تغذیه ای بالا است. همانطور که اشاره شد حرارت ناکافی و یا حرارت بیش از حد هر دو منجر به یک کنجاله سویا با کیفیت پایین خواهد شد. بنابراین تولید کنندگان خوراک نیازمند روش هایی برای تشخیص فرآوری حرارتی کافی و بهینه کنجاله سویا هستند.
کیفیت کنجاله سویا به دو پارامتر وابسته است:
۱: کاهش فاکتورهای ضد تغذیه ای
۲: بهینه ساختن قابلیت هضم پروتئین
تولیدکنندگان کنجاله سویا و مصرف کنندگان آن ها در صنعت تولید خوراک نیازمند روش های قابل اعتماد، سریع و با صرفه اقتصادی هستند. از آنجایی که آنالیز های مستقیم هر دوی این پارامتر ها زمان بر و سخت می باشد، با استفاده از روش های جایگزین با آزمون های غیر مستقیم مانند شاخص اوره آز (UI)[4]، شاخص تفرق پروتئین (PDI)[5]، حلالیت پروتئین در پتاسیم هیدروکسید (PS)[6]، قابلیت هضم پروتئین، تعیین میزان لیزین فعال و روش اسپکترومتری NIR[7] کیفیت کنجاله سویا مورد ارزیابی قرار می گیرد. بنابراین هدف از این تحقیق مقایسه برخی از روش های آزمایشگاهی (in-vitro) به منظور بررسی کیفیت کنجاله سویا در رابطه با میزان فرآوری پایین یا بالا می باشد.
اندازه گیری پروتئین خام کنجاله سویا (CP)[8]
میزان پروتئین در کنجاله سویا بسته به عوامل متغیری وابسته می باشد. به عنوان مثال کیفیت واریته سویا، زمان برداشت و مکان کشت از جمله عوامل مهم در تعیین میزان پروتئین خام کنجاله سویا است. میزان پروتئین خام در آزمایشگاه به صورت روتین با استفاده از روش کجلدال انجام می شود اما از آنجایی که این شاخص صرفاً یک شاخص کمی بوده و هیچ گونه اطلاعاتی از کیفیت پروتئین موجود درکنجاله سویا را برآورد نمی کند نمی توان آن را به عنوان یک روش جامع و کامل از کیفیت سنجی کنجاله سویا در نظر گرفت.
شاخص اوره آز (UI)
هدف اولیه از اندازه گیری این شاخص به منظور تعیین میزان حرارت کافی و تجزیه بیشتر فاکتور های ضدتغذیه ای است. دانه و کنجاله سویا هر دو حاوی آنزیم اوره آز هستند. اوره آز آنزیمی است که اوره را هیدورلیز کرده و تولید کربن دی اکسید و آمونیاک می کند. تولید آمونیاک منجر به افزایش pH محلول می شود. تجزیه ساختار اوره آز به وسیله حرارت بسیار مرتبط و نزدیک به تجزیه بازدارنده تریپسین و دیگر فاکتور های ضدتغذیه ای می باشد. محدوده pH شاخص اوره آز بین ۰/۰۵ تا ۰/۲ است و مقادیر بالاتر از ۰/۲ بیانگر حرارت کم و مقادیر کمتر از ۰/۰۵ نشان دهنده حرارت بیش از حد می باشد. بر اساس برخی از رفرنس ها محدوده ۰/۰۵ تا ۰/۳ نیز محدوده قابل قبول گزارش شده است. محققان گزارش کرده اند که این روش یک روش مناسب جهت تشخیص فرآوری حرارتی پایین در کنجاله سویا می باشد و در رابطه با کنجاله های سویایی که بیش از حد حرارت دیده باشند محدودیت هایی دارد (۱۱).
حلالیت پروتئین در پتاسیم هیدروکسید (PS)
حلالیت پروتئین در پتاسیم هیدروکسید از جمله شاخص هایی است که اطلاعات ضد و نقیضی در رابطه با کارایی آن برای سنجش کیفیت کنجاله های سویا با حرارت بالاتر و پایین تر از حد اپتیمم وجود دارد. با این حال این شاخص در محدوده بین ۷۸ تا ۸۴ درصد به عنوان یک محدوده مناسب به منظور حرارت دهی بهینه در نظر گرفته می شود. حرارت باعث کاهش حلالیت پروتئین می شود. بنابراین مقادیری در محدوده ۸۴ تا ۸۹ درصد نشان دهنده فرآوری پایین بوده که ممکن است برای بیشترحیوانات قابل قبول باشند اما در مقابل مقادیر پایین تر از ۷۴ درصد نشان دهنده فرآوری حرارتی بالا کنجاله سویا بوده و ممکن است قابلیت هضم لیزین در آن پایین باشد.
شاخص تفرق پروتئین (PDI)
شاخص تفرق پروتئین یکی دیگر از روش های مورد استفاده به منظور بررسی کیفیت پروتئین کنجاله سویا می باشد. این روش در واقع مخلوط کردن نمونه و آب با استفاده از یک میکسر قوی است. داده های آزمایشگاهی به دست آمده حاکی از آن است که این شاخص بسیار حساس تر از شاخص اوره آز و حلالیت پروتئین برای تعیین میزان اپتیمم فرآوری حرارتی در کنجاله سویا است. با این حال هیچ کدام از شاخص ها به تنهایی نمی تواند معیار کاملی از کیفیت کنجاله سویا باشد و بنابراین ترکیب این معیارهای بررسی با یکدیگر و حصول یک نتیجه درست مدنظر می باشد.
به عنوان مثال کنجاله سویا حاوی اوره آز پایین (۰/۳ یا پایین تر) و PDI بالا (۴۰ تا ۴۵ درصد) ممکن نشان دهنده کیفیت بالا با میزان کافی از حرارت دهی باشد. اگرچه در آزمایشی که توسط برخی از محققان بر روی میزان رشد جوجه های گوشتی انجام شده بود گزارش شده است که هیچ تفاوتی بین کنجاله ای که در حد بهینه حرارت دیده است و کنجاله سویا با میزان حرارت دهی بالا در میزان دسترسی زیستی پروتئین مشاهده نشد. بنابراین پیشنهاد می شود که PDI روش درستی برای قابلیت دسترسی زیستی اقلام خوراک از جمله کنجاله سویا نمی باشد (۱۲).

قابلیت هضم آنزیمی پروتئین
روش قابلیت هضم آنزیمی به وسیله یکی از آنزیم های دستگاه گوارش از جمله پپسین یکی از روش های گسترده مورد استفاده برای ارزیابی کیفیت پروتئین کنجاله سویا می باشد. این روش یک روش تک آنزیمی بوده که توسط بسیاری از محققان مورد ارزیابی قرار گرفت. در این ارزیابی ها همبستگی حدود ۰/۹۱ برای قابلیت هضم توسط پپسین با پروتئین قابل استفاده در جوجه های گوشتی گزارش شد. در یک روش دیگر از قابلیت هضم آزمایشگاهی، استفاده از پانکراتین به عنوان یک روش جدید جهت قابلیت هضم پروتئین مورد بررسی قرار گرفت.
در بین محققان نتایج متفاوتی از راندمان متفاوت این دو روش دیده می شود در این راستا برخی از محققان روش استفاده از آنزیم پانکراتین را قابل اعتماد تر گزارش کرده اند و برخی از محققان تفاوتی را بین دو روش قائل نشده و هر دو روش را یکسان دانسته اند. در نهایت قابلیت هضم پپسین-پانکراتین (روش چند آنزیمی) به عنوان یک روش قابل اعتماد تر با همبستگی بالا بین قابلیت هضم پروتئین در حیوان و قابلیت هضم آزمایشگاهی با استفاده از روش پپسین- پانکراتین به دست آمد (۱۲).
اندازه گیری لیزین فعال
لیزین فعال، لیزینی است که در معرض واکنش میلارد قرار نگرفته و به دلیل اینکه دارای یک گروه آمین آزاد در زنجیره جانبی می باشد می تواند در ساختار پروتئین شرکت کند. در مقابل لیزینی که گروه آمین آن متصل با قندها می باشد به عنوان لیزین غیرفعال است. لیزین فعال با چندین نام دیگر نیز خوانده می شود از جمله لیزین فعال شیمیایی، لیزین فعال قابل دسترس، لیزین قابل دسترس و لیزین قابل دسترس کل. اندازه گیری آزمایشگاهی لیزین کل خوراک شامل هیدرولیز اسیدی پروتئین های موجود در کنجاله سویا است که به عنوان روش های فوروزین و روش هوموآرژنین شناخته می شود (۱۳).
روش فوروزین
با استفاده از روش فوروزین محتوای لیزین فعال بر اساس غلظت فوروزین در کنجاله سویا مورد بررسی قرار می گیرد. فوروزین آمینو اسیدی است که پس از هیدرولیز اسیدی محصولات آمادوری که در اثر واکنش میلارد با تعامل گروه های آمینو لیزین با گلوکز ، لاکتوز یا مالتوز ایجاد می شود بوجود می آید. بنابراین فوروزین به عنوان شاخص مفیدی از میزان پروتئین های آسیب دیده در طی واکنش میلارد در کنجاله سویا می باشد (۱۳).
روش هوموآرژنین
از روش هموآرژینین، که طی آن تبدیل لیزین فعال به هموآرژینین اتفاق می افتد، می توان برای تعیین لیزین فعال استفاده کرد. در واکنش گوانیداسیون، لیزینی که به قندها متصل نیست به هموآرژینین تبدیل می شود. هنگامی که از روش هموآرژین استفاده می شود، محتوای لیزین فعال بر اساس مقدار هموآرژینین تشکیل شده در طی واکنش گوانیداسیون، تعیین می شود. هموآرژینین در محیط اسیدی پایدار است، بنابراین محتوای آن در پروتئین پس از هیدرولیز اسیدی نشان دهنده لیزین فعال می باشد. در طی تجزیه و تحلیل اسید های آمینه در روش کروماتوگرافی، تمایز بین لیزین فعال و غیرفعال ایجاد می شود، زیرا لیزین فعال به صورت هموآرژینین و لیزین بازسازی شده به صورت لیزین ظاهر می شود (۱۳).
با این حال گزارش شده است که در طی هیدرولیز اسیدی برخی از لیزین های آسیب دیده می توانند آزاد شده و به عنوان لیزین فعال در نظر گرفته شوند که این نوع لیزین قابلیت متابولیسم برای حیوان ندارد و تخمین نادرستی از لیزین فعال بیولوژیکی را باعث خواهد شد.
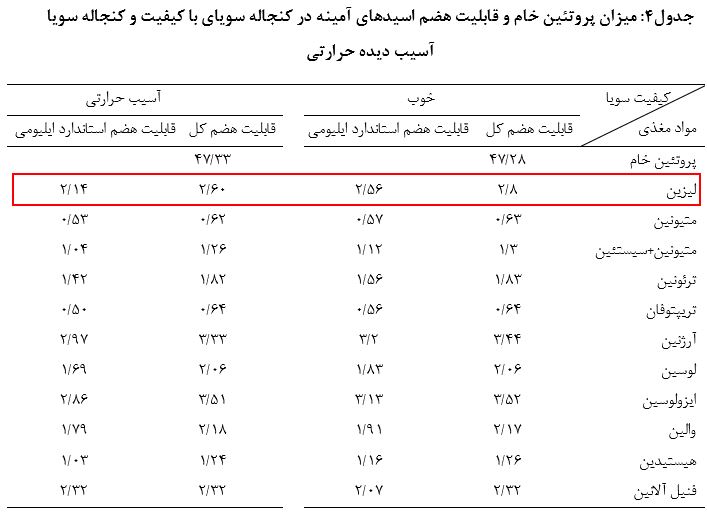
لیزین فعال قابل متابولیسم ایلیومی
برای تشخیص لیزینی که می تواند توسط حیوان هضم و متابولیزه شود، لیزین فعال قابل متابولیسم ایلیومی باید تعیین شود. حرارت به طور خطی محتوای لیزین کل را از ۲۷/۵ به ۱۹/۲ و لیزین فعال را از ۲۳/۴ به ۱۱/۷ گرم به ازای کیلوگرم کنجاله سویا کاهش می دهد. قابلیت هضم ظاهری، واقعی و استاندارد ایلیومی لیزین و لیزین فعال شاخص های درست تری در مقایسه با برآورد لیزین کل و لیزین فعال در کنجاله های سویایی که درمعرض حرارت قرار گرفته اند می باشد. اگرچه این روش یک روش invivo (مطالعه بر روی حیوان) می باشد اما تخمین درست تری از میزان لیزین فعال را برآورد می کند (۱۴).
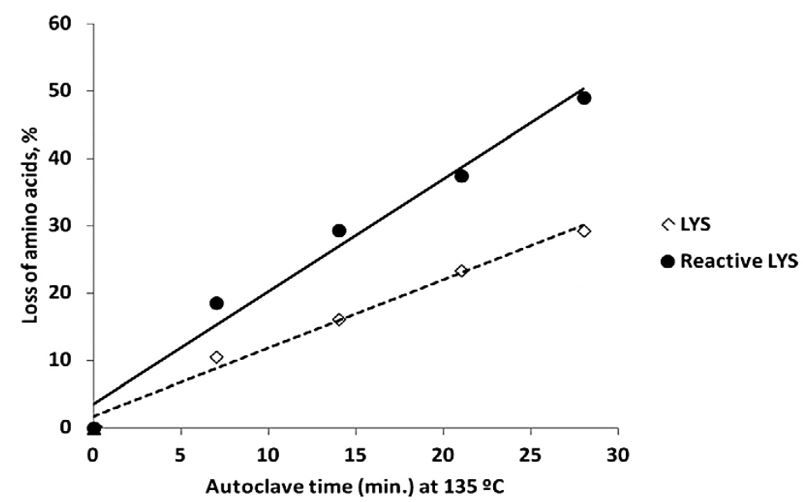
نمودار ۱: بررسی میزان اسید آمینه لیزین کل و لیزین فعال با افزایش زمان اتوکلاو
روش اسپکتروسکوپی NIR
یکی از روش هایی که اخیراً به شدت مورد توجه متخصصین تغذیه قرار گرفته است روش NIR می باشد. از آنجایی که بیشتر روش های آزمایشگاهی در رابطه با سویا هایی که بیش از حد و یا کمتر از حد بهینه حرارت دیده باشند مناسب نبوده و در اکثر مواقع باید چندین آزمایش کیفی جهت حصول یک نتیجه درست تر انجام شود، استفاده از روش NIR روشی سریع و با صرفه اقتصادی و در عین حال قابل اعتماد تر معرفی شده است. شایان ذکر است که در اختیار داشتن رفرنس یا بانک اطلاعاتی معتبر و همچنین اطلاع درست از منبع خوراک مورد آزمایش یکی از مهمترین فاکتورهای رسیدن به آنالیز واقعی خوراک در این روش می باشد. در تحقیقاتی که اخیراً محققان بر روی همبستگی بین داده های به دست آمده از آزمایشگاه و NIR انجام داده اند حاکی از آن است که همبستگی بین این دو دسته از داده ها در رابطه با لیزین، لیزین فعال و نسبت آن با پروتئین بالا است اما در رابطه با میزان پروتئین خام این دو دسته از داده ها همبستگی بسیار پایینی را نشان داد (نمودار۲) (۱۵).
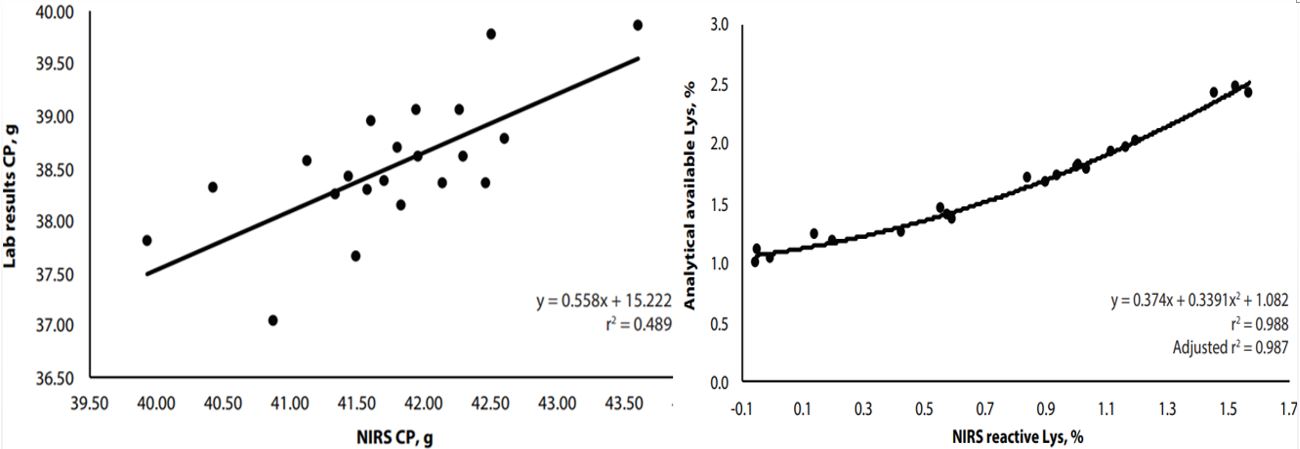
نمودار۲: تفاوت همبستگی بین داده های آزمایشگاهی و NIR محتوای پروتئین خام (سمت چپ) و نسبت لیزین به پروتئین (سمت راست)
رفرنس ها
- Lagos L, Stein H-H. Chemical composition and amino acid digestibility of soybean meal produced in the United States, China, Argentina, Brazil, or India. Journal of animal science. 2017;95(4):1626-36.
- Dei H. Soybean as a feed ingredient for livestock and poultry: INTECH Open Access Publisher; 2011.
- Wedekind KJ, Chen J, Yan F, Escobar J, Vazquez-Anon M. Efficacy of a mono-component protease is affected by trypsin inhibitor concentration in soybean meal. Animal Feed Science and Technology. 2020:114502.
- Dozier W, Hess J, El-Shemy H. Soybean meal quality and analytical techniques. Soybean and Nutrition InTech Publishing, Rijeka, Croatia. 2011:111-24.
- He L, Han M, Qiao S, He P, Li D, Li N, et al. Soybean antigen proteins and their intestinal sensitization activities. Current Protein and Peptide Science. 2015;16(7):613-21.
- Valentine MF, De Tar JR, Mookkan M, Firman JD, Zhang ZJ. Silencing of soybean raffinose synthase gene reduced raffinose family oligosaccharides and increased true metabolizable energy of poultry feed. Frontiers in Plant Science. 2017;8:692.
- Chen X, Parsons CM, Bajjalieh N. Nutritional evaluation of new reduced oligosaccharide soybean meal in poultry. Poultry science. 2013;92(7):1830-6.
- Banaszkiewicz T. Nutritional value of soybean meal. Soybean and nutrition. 2011:1-20.
- Nahavandinejad M, Seidavi A, Asadpour L. Effects of soybean meal processing method on the broiler immune system. Kafkas Univ Vet Fakultesi Dergisi 2012a. 2012;18(6):965-72.
- Mathai J, Htoo J, Wiltafsky M, Stein H. 47 Effects of Various Heat Treatments on Concentrations of Digestible and Metabolizable Energy and on Amino Acid Digestibility in Soybean Meal Fed to Growing Pigs. Journal of Animal Science. 2018;96(suppl_2):25-6.
- Caprita R, Caprita A, Gheorghe I, Cretescu I, Simulesku V, editors. Laboratory procedures for assessing quality of soybean meal. Proc World Congress on Engineering and Computer Science, WCECS; 2010: Citeseer.
- Bryan DD, Classen HL. In Vitro Methods of Assessing Protein Quality for Poultry. Animals. 2020;10(4):551.
- Brestenský M, Nitrayová S, Heger J, Patráš P, Rafay J, Sirotkin A. Methods for determination reactive lysine in heat-treated foods and feeds. Journal of Microbiology, Biotechnology and Food Sciences. 2020;9(4):13-5.
- Kim J, Mullan B, Pluske J. Prediction of apparent, standardized, and true ileal digestible total and reactive lysine contents in heat-damaged soybean meal samples. Journal of Animal Science. 2012;90(suppl_4):137-9.
- Dunmire K, Dhakal J, Stringfellow K, Stark C, Paulk C. Evaluating Soybean Meal Quality Using Near-Infrared Reflectance Spectroscopy. Kansas Agricultural Experiment Station Research Reports. 2019;5(8):34.
[۱] Anti-Nutritive Factors
[۲] High protein soybean meal
[۳] Conventional soybean meal
[۴] Urease activity index
[۵] Protein dispersible index
[۶] Potassium hydroxide solubility
[۷] near-infrared reflectance spectroscopy
[۸] Crud protein
کنجاله سویا در تغذیه طیور